基于内增强TiO2纳米管阵列的高效电化学flow-through阳极的研制


第一作者:陈敏
通讯作者:王灿教授(wangcan@tju.edu.cn)
通讯单位:天津大学
DOI:https://doi.org/10.1016/j.envint.2020.105813
期刊名称:Environment International
研究背景:
电化学高级氧化法(EAOPs)因其结构简单、操作方便、可扩展性强、在降解非生物降解污染物方面的有效性被认为是一种很有前途的水处理技术。阳极可产生羟基自由基(HOradical-dot),羟基自由基对多种难降解有机污染物具有优异的降解能力。尺寸稳定阳极(DSA)是EAOPs中应用最广泛的电极材料之一,但传统的操作方式传质性能差,能耗高。这是由于流动模式中较低的传质速率和泰勒色散,因为污染物和羟基自由基之间的反应只发生在阳极表面的狭窄区域(<1μm),但在流动模式下,阳极表面的扩散边界层厚度大于100μm。
近年来,一些研究集中于基于多孔结构阳极的EAOPs设计,其孔径与反应边界层相当。因此,flow-through式阳极增强了传质和羟基自由基与目标化合物的反应。先前报告的多孔阳极材料包括Ti4O7、Ti/PbO2、Ti/RuO2和Ti/SnO2-Sb2O3。然而,一些挑战限制了它们的应用。例如,Magneli相TinO2n-1表现出优于普通材料的降解性能,但需要较长的还原合成时间(50小时),并且需要在一定压力下操作。Ti/PbO2具有稳定的电化学性质,但是存在释放重金属离子的风险。Ti/RuO2受到低析氧过电位(OEP)的限制,Ti/SnO2-Sb2O3不稳定且寿命短。因此,有效的多孔阳极需要进一步发展。
根据先前的研究,TiO2纳米管阵列(NTAs)具有良好的电子传输性能、大的带隙(△E=3.2eV)、以及对于导电带电子(e−cb)和价带孔(h+)的低复合速率,改善了阳极表面羟基自由基的产生。此外,TiO2 NTAs可提高OEP,从而抑制电解过程中的副反应。此外,TiO2-NTAs可以有效地改善具有有序堆积结构的SnO2-Sb2O3层的电化学性能。此外,TiO2 NTA可提高OEP,从而抑制电解过程中的副反应。此外,TiO2-NTAs可以有效地改善具有有序堆积结构的SnO2-Sb2O3层的电化学性能。因此,TiO2 NTAs延长了阳极的使用寿命。然而,NTAs的制备需要进一步改进,因为NTAs传统上是在含氟电解液中制造的,该电解液可产生富氟TiO2层。这种方法导致Ti基板和NTA之间的界面结合较弱。根据先前的研究,NTA的结构强度可通过使用H3PO4/PEG溶液的第二次阳极氧化来提高,形成额外的致密层,从而在合成过程中消除富氟TiO2层。上述策略增强了NTA与Ti基板的结合。此外,NTA的导电性较低,但可通过阴极化改善其与涂层的进一步结合。在本研究中,我们通过在大孔钛基板内生长增强型NTA(ENTA)来制造一种新的大孔流动阳极。然后,我们用SnO2-Sb2O3覆盖ENTA。新型大孔阳极被称为MP-Ti-ENTA/SnO2-Sb2O3阳极。
采用常见的生物杀伤剂2-甲基-4-异噻唑啉-3-酮(MIT)作为目标污染物。选择MIT是因为其具有毒性风险且不易生物降解。研究了电极的标称孔径、电极厚度、电流密度、初始浓度、电解液浓度和电极间距等关键参数。测定了自由基和非自由基氧化对MIT降解的贡献。此外,我们还评估了电流效率和能量消耗,并我们的MP-Ti-ENTA/SnO2-Sb2O3阳极与其他阳极和各种AOPs进行了比较。
文章亮点:
1.通过电化学工艺制备了一种新型的强化大孔阳极
2.该阳极具有优良的电化学性能和降解性能
3.为进一步设计多孔阳极,对flow-through式阳极的优化进行了研究
4.定量分析了自由基氧化和非自由基氧化对降解的贡献
5.研究了MIT降解的能量效率比较
文章总结:
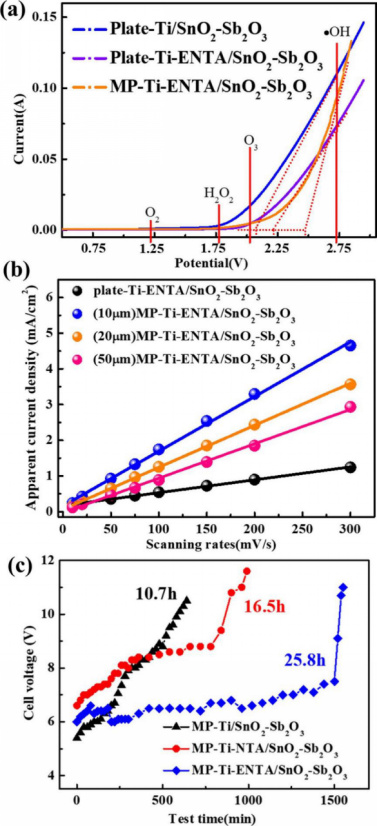
图4 平板Ti/SnO2-Sb2O3、Ti-ENTA/SnO2-Sb2O3和MP-Ti-ENTA/SnO2-Sb2O3(平板Ti:无孔Ti箔)的电化学性能,(a)Ti/SnO2-Sb2O3、Ti-ENTA/SnO2-Sb2O3和MP-Ti-SnO2-Sb2O3阳极在0.5 mV H2SO4溶液中的LSV曲线,扫描速率为50 mV s−1,(b) Ti-ENTA/SnO2-Sb2O3和MP-Ti-ENTA/SnO2-Sb2O3阳极在不同扫描速率(10–300 mv s−1,0.1 M Na2SO4,表面面积19.625 cm2)下1.0 V vs.SCE的表观电流密度,(c)电极加速使用寿命试验(外加电流:2A,表面积:4 cm2,0.5 M H2SO4溶液,标称孔径:50μM)。
图4显示了不同电极的LSV和电流密度曲线。图4a示出用于平板Ti/SnO2-Sb2O3电极、平板Ti ENTA/SnO2-Sb2O3和MP-Ti-ENTA/SnO2-Sb2O3的oep分别约为2.05 V(相对于NHE)、2.24 V(相对于NHE)和2.48 V(相对于NHE)。中间TiO2 NTA层的主要优点是阳极OEP增加。此外,多孔结构也有助于增加氧空位并改善OEP。具有高OEP(和大的带隙)的阳极具有足够的能量来阻止氧的释放并有利于HO·的产生。
图4b表明,通过比较电极的电容和光滑电极的电容,可以通过电流密度曲线的斜率来计算粗糙系数Rf。孔径为10、20和50μm的MP-Ti-ENTA/SnO2-Sb2O3的Rf值分别为255.3、196.5和160.7。因此,多孔阳极的Rf值高于平板电极的Rf值(60.2),表明与平板阳极相比,多孔阳极的表面积增大。此外,MP-Ti-ENTA/SnO2-Sb2O3、MP-Ti-NTA/SnO2-Sb2O3、MP-Ti-NTA/SnO2-Sb2O3电极的加速使用寿命试验如图4c所示,其加速使用寿命分别为25.8、16.5和10.7小时。由于NTA的存在,MP-Ti-NTA/SnO2-Sb2O3电极的使用寿命比MP-Ti/SnO2-Sb2O3电极延长了1.54倍。此外,经过两个阳极化步骤和一个生成增强型TiO2纳米管内层的阴极化步骤后,MP-Ti-ENTA/SnO2-Sb2O3的使用寿命长于MP-Ti-NTA/SnO2-Sb2O3。根据相关研究,NTA的电阻因阴极化步骤而急剧降低。此外,Ti-ENTA/SnO2-Sb2O3的电化学性能比Ti-NTA/SnO2-Sb2O3更稳定。内层良好的导电性有助于抑制电解过程中的电压升高。结果表明,增强的TiO2纳米管内层导电性延长了阳极寿命。相应地,多孔阳极的稳定性提高。
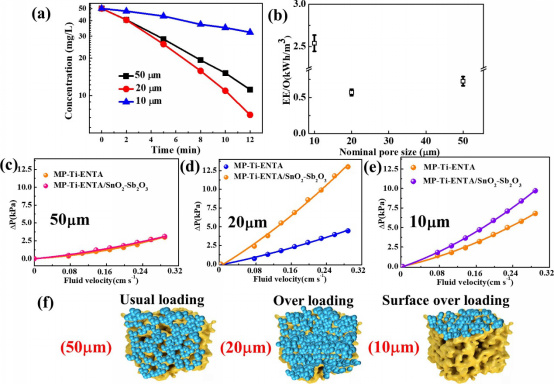
图5 孔径对电化学flow-through系统的影响(电极厚度:3 mm),(a)MIT去除效率(表观电流密度:5 mA cm−2,面部面积:19.625 cm2,MIT浓度:50 mg L−1),(b)能量效率,(c)标称孔径为50μm时的压降曲线,(d) 标称孔径为20μm时的压降曲线;(e)标称孔径为10μm时的压降;(f)不同孔径下SnO2-Sb2O3涂层加载的可能机理。
对于10、20和50μm的标称孔径,电极的表观速率常数分别为0.38、1.63和1.24 min−1(图5a)。图5b显示了不同标称孔径的EE/O值为2.5 kWh m−3至0.7 kWh m−3。上述结果似乎与多孔基底空隙的比表面积不一致,因为多孔基底的大比表面积可以为氧化提供更多的反应位点。图5c-e显示了不同孔径的压降。随着流体速度的增加,压降逐渐增大。加载涂层后,10μm、20μm和50μm MP Ti ENTA标称孔径的压降变化(ΔP)分别为2.9、8.5和0.2 kPa,流速为0.30 cm s−1。此外,10μm、20μm和50μm标称孔径的MP-Ti-ENTA在加载混合金属氧化物层后的压降分别增加了42%、192%和3%。这一现象的可能解释如图5f所示。由于老化的SnO2-Sb2O3溶胶-凝胶具有高粘度,在加载涂层过程中,具有小孔径(10–20μm)的电极出现表面和内部堵塞。因此,当孔径较小时,会发生过载。与预期的一样,当多孔电极被SnO2-Sb2O3包覆时,较大孔径(50μm)的压降变化较小。老化溶胶-凝胶的堵塞状况阻碍了内部反应位点(约10μm多孔基底)的有效和充分利用。这一结果表明,催化层在多孔电极上的负载必须通过压力比较来优化,以充分利用内部反应位点,并综合考虑额外的泵送费用和催化剂损失。
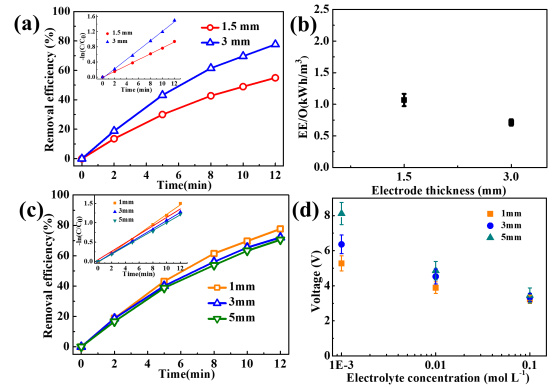
图S4. 电极厚度和间距对电化学流动的影响,(a)不同厚度的MIT去除效率,(b)不同阳极厚度的能量效率,(c)阳极和阴极间距的MIT去除效率,以及(d)不同电解质浓度下的观察电压。(流速=0.08 cm s-1,外加电流=100 mA,电解液浓度:0.1 M Na2SO4,标称孔径=50μM,体积=150 mL)
厚阳极可促进MIT在电化学flow-through系统中的降解。随着阳极厚度从1.5 mm增加到3.0 mm,MIT速率常数从0.77 min−1增加到1.24 min−1。如图S4b所示,EE/O值从1.1 kWh m−3变为0.7 kWh m−3。随着阳极厚度的增加,多孔阳极内表面的反应位点逐渐增多,说明增大的比表面积可以提高多孔阳极的降解性能。在流动阳极流速较低(0.08cms−1)下,降解性能主要受传质过程控制。因此,观察到的速率常数受不同阳极厚度的影响。图S4c显示,随着阳极和阴极之间的电极间距的增加,MIT降解效率没有显著提高。此外,电解液浓度对保持相同电流密度所需的外加电压有显著影响(图S4d)。特别是在电极间距为5mm的条件下,随着电解液浓度从0.1m降低到0.001m,电压由3.5v增加到8.1v,增加了能耗。
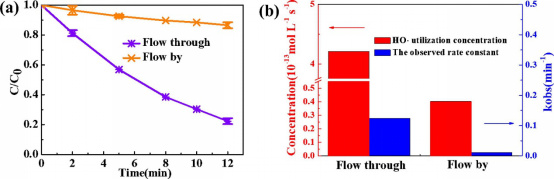
图6 flow-by和flow-through系统的MIT降解比较.(a) flow-through和flow-by系统的MIT降解性能(b)稳态羟基自由基利用浓度和flow-through和flow-by系统的观察反应速率。(施加电流:100 mA,电极间距:3 mm,MIT浓度:50 mg L−1,pCBA浓度夹带:2000μg L−1,支持电解质:0.1 mol L−1 NaClO4,通量:98 mL min−1)。
在相同的电流值下,flow-through系统的氧化效率优于flow-by系统。经过12分钟的电解后,flow-through模式下的MIT降解效率约为80%,而通过flow-by系统的MIT降解效率为11%。2-羟基对苯二甲酸的荧光强度与电化学氧化过程中羟基自由基的产生呈线性关系。因此,可以使用pCBA作为探针(kHO•/pCBA=5.0×109 M−1 S−1)计算羟基自由基稳态浓度,如图6b所示。理论上,羟基自由基浓度与电子流之间存在比例关系。在相同的电流条件下,比较flow-by和flow-through阳极的稳态浓度可以用来评价传质效率。电化学flow-through模式(4.21×10−13 mol L−1 s−1)的稳态时间点浓度是按flow-by模式流动(0.40×10−13 mol L−1 s−1)的10.3倍,表明该流动系统将更快速有效地氧化目标有机物。这一发现与系统观察到的反应速率常数一致,即flow-through阳极和flow-by阳极的反应速率常数分别为0.124min−1和0.0118min−1。
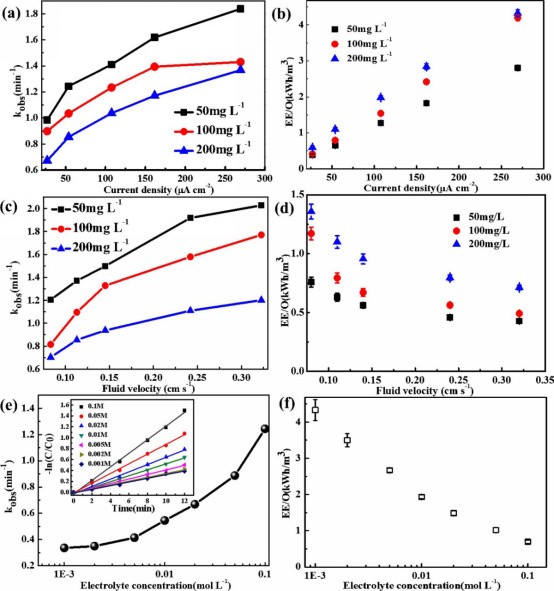
图7 操作条件对MIT降解的影响:(a)各种电流密度(流速:0.08 cm s−1)的观测速率常数,(b)各种视在电流密度下的EE/O,(c)各种速度下的观测速率常数(实际电流密度:53.8μa cm−2),(d)各种速度下的EE/O,(e)观察到的速率各种电解液浓度恒定,(f)不同电解液浓度下的EE/O(电极间距=1 mm,标称孔径=50μm,储液罐容积=150 mL)。
如图7a所示,对于100 mg L−1的初始MIT浓度,观察到的速率常数随着电流密度的增加从0.91 min−1增加到1.35 min−1。对于50和200 mg L−1的初始浓度,也观察到类似的结果。高电流密度增加了空穴和导带电子的产生,产生了更多的羟基自由基,从而提高了MIT的氧化速率。如图7b所示,当电流密度从26.9μA cm−2增加到269.4μA cm−2时,EE/O从0.35 kWh m−3增加到4.25 kWh m−3。此外,我们发现电流密度与EE/O呈线性关系。一般来说,在低电流密度和低EE/O的条件下,电化学氧化反应具有较高的效率,并且可以充分利用羟基自由基。
此外,我们还研究了流体通过多孔电极的速度对MIT氧化速率的影响。如图7c所示,在初始MIT浓度为50 mg L−1时,随着流体速度从0.08 cm s−1增加到0.32 cm s−1,观察到的反应速率常数从1.24 min−1增加到2.24 min−1。在100 mg L−1和200 mg L−1的初始浓度下,观察到类似的速率常数增长趋势。如图7d所示,在0.08 cm s−1到0.32 cm s−1的流体速度范围内,初始MIT浓度为200 mg L−1时,EE/O从1.35 kWh m−3降低到0.75 kWh m−3。随着流速的增加,50 mg L−1和100 mg L−1的EE/O下降趋势相似。根据Gnielinski相关性(Critenden et al.,2012),流速与雷诺数或传质系数之间存在正相关关系,即增大流体流速也会增强传质过程。
图7e–f显示了电解液(Na2SO4)浓度对MIT降解的影响。随着硫酸钠浓度的增加,观察到的MIT降解速率常数从0.32 min−1逐渐增加到1.24 min−1。一些研究报告说,高硫酸盐浓度下可能会生成过硫酸盐,这会增加硫酸盐自由基的生成。随着电导率从0.001 M增加到0.1 M Na2SO4电解液,高电解液浓度可以增加从阳极到阴极的电子流,这两种效应都会增加MIT氧化速率。如图7f所示,当硫酸盐电解液浓度从0.001 m增加到0.1 m时,EE/O从4.35 kWh m−3降低到0.75 kWh m−3。
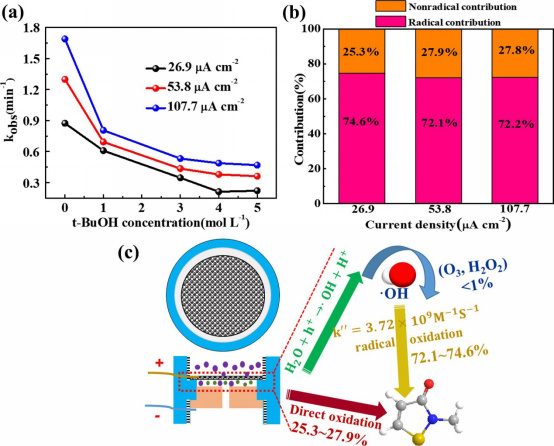
图8 自由基或非自由基氧化的降解贡献。(a) 添加t-buOH对MIT降解的影响(支持电解质:0.1 M NaClO4,MIT浓度:50 mg L−1,流速:0.08 cm s−1,标称孔径=50μM,体积=150 mL),(b)电流密度对自由基和非自由基氧化降解贡献的影响,以及(c)MIT降解贡献的示意图。
图8a显示了在不同的实际电流密度(表观值在50毫安到200毫安之间)下添加t-buOH对MIT降解的影响。随着t-buOH浓度的增加,在107.7μa cm−2电流密度下,观察到的一级反应速率从1.68 min−1降低到0.47 min−1。初始浓度为26.9和53.8μA cm−2时也观察到类似的结果。根据这些结果,可以计算出非自由基和自由基氧化对MIT降解的贡献,如图8b–c所示。在26.9–107.7μA cm−2(外加电压:2.8–3.9 V)的电流密度范围内,自由基氧化约占72.1%–74.8%,非自由基氧化占MIT氧化的25.2%~26.1%。此外,其他氧化剂(O3、H2O2)的单独贡献可忽略不计。
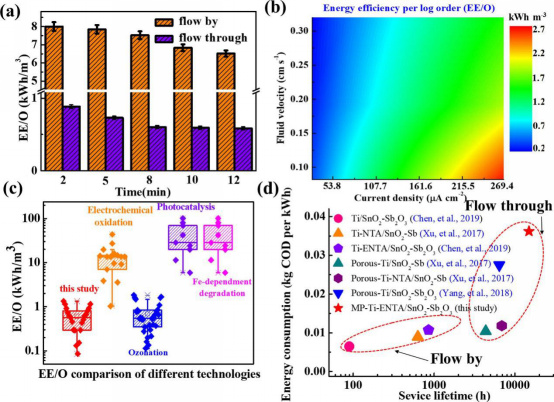
图9 flow-through和flow-by阳极的能耗评估。(a)flow-through和flow-by系统之间的EE/O比较(MIT浓度:50 mg L−1,流速:0.08 cm s−1,外加电流:100 mA,阳极横截面积:10 cm2),(b)不同流速和电流密度下的EE/O评估(MIT浓度:50 mg L−1),(c) AOP之间的EE/O比较(计算操作能耗时忽略了泵送和磁搅拌能耗),(d)各种阳极的能耗(换算表观电流密度:20 mA cm−2)。
图9a所示,flow-through(~0.58 kWh m−3)的EE/O值比flow-by阳极(约6.85 kWh m−3)低得多。图9b显示了不同流体速度和电流密度的EE/O值通过Runge–Kutta插值进行优化,并用于进一步分析流动系统的能量效率。高电流密度和高流速下,过流阳极的MIT降解加剧。然而,电流密度的相应增加也导致了EE/O的增加。模拟等值线数据表明,为了节约能源,有机降解的电流密度不应超过80.7μA cm−2。
根据之前的研究,图9c展示了MIT降解的各种高级氧化技术的EE/O值。因此,flow-through阳极和臭氧氧化具有最低的EE/O(0.24–1.83 kWh m−3)。一般情况下,过滤方式的泵能也占到了运行成本的一部分。然而,泵送能量消耗可以忽略,因为它只占运行能耗的一小部分。图9d总结了各种阳极和不同操作模式对COD降低的能耗。结果表明,以kg-COD/kWh计,flow-through系统对有机物的破坏效率高于flow-by系统。此外,TiO2 NTA中间层结构和多孔基底可显著提高阳极的使用寿命和降解性能。MP-Ti-ENTA/SnO2-Sb的转化寿命达到16125h(20mAcm-2),是多孔Ti-NTA/SnO2-Sb阳极的2.48倍。这些结果表明,通过使用ENTA作为中间层(使用两个阳极化和阴极化步骤)可以显著改善。我们还研究了不同类型的过流阳极的能效和去除性能,这些阳极在降解有机污染物方面表现出低能耗(0.084–6.7 kWh m−3)。进一步验证了该反应模式具有很大的实际应用潜力。
在本研究中,我们利用溶胶-凝胶法,在不同标称孔径的多孔钛上原位生长了一种新型的大孔Ti-ENTA/SnO2-Sb2O3(MP-Ti-ENTA/SnO2-Sb2O3)阳极。以常用杀菌剂MIT为目标污染物,研究了MP-Ti-ENTA/SnO2-Sb2O3阳极在电化学流动系统中的参数优化、机理及能耗评估。
阳极具有较高的析氧过电位(2.48v),抑制析氧并产生许多羟基自由基。值得注意的是,ENTA层提高了MP-Ti-ENTA/SnO2-Sb2O3的加速使用寿命,是MP-Ti-NTA/SnO2-Sb2O3的1.56倍。此外,MP-Ti(10μm)-ENTA/SnO2-Sb2O3、MP-Ti(20μm)-ENTA/SnO2-Sb2O3和MP-Ti(50μm)-ENTA/SnO2-Sb2O3的伪一级速率常数分别为0.38、1.63和1.24 min-1。实验结果揭示了不同孔径多孔钛基底的催化层负载机制。
自由基清除实验表明,羟基自由基是MIT氧化的优势物种。我们测定了72.1%-74.8%的羟基自由基贡献和25.1%-27.8%的直接电子转移对MIT氧化的贡献。其他氧化剂,如H2O2和O3,对MIT的氧化贡献小于1%。最后,我们比较了MIT氧化的各种先进氧化技术,发现flow-through阳极的EE/O为0.58 kWh m−3,低于flow-by阳极流动的6.85 kWh m−3 EE/O,说明了flow-through阳极优于flow-by阳极。